May -Akda:
Frank Hunt
Petsa Ng Paglikha:
13 Marso. 2021
I -Update Ang Petsa:
1 Hulyo 2024

Nilalaman
- Upang humakbang
- Paraan 1 ng 3: Paggamit ng isang meter ng pH
- Paraan 2 ng 3: Sa litmus paper
- Paraan 3 ng 3: Pag-unawa sa PH
Mahalagang sukatin ang ph - ang antas ng kaasiman o alkalinity - ng tubig. Ang tubig ay ginagamit ng mga halaman at hayop na umaasa, at iniinom natin ito araw-araw. Ang halaga ng ph ng tubig ay maaaring maging isang pahiwatig ng posibleng kontaminasyon, kaya't ang pagsukat ng ph ng tubig ay maaaring maging isang mahalagang pag-iingat sa kalusugan ng publiko.
Upang humakbang
Paraan 1 ng 3: Paggamit ng isang meter ng pH
 I-calibrate ang pagsisiyasat at metro ayon sa mga tagubilin sa pabrika. Maaaring kailanganin mong i-calibrate ang metro gamit ang isang sangkap na may kilalang halaga ng PH. Ang metro ay maaaring iakma ayon sa sangkap na iyon. Kung susubukan mo ang tubig sa labas ng isang lab, inirerekumenda na isagawa mo ang pagkakalibrate na ito ng ilang oras bago ang pagsubok sa bukid.
I-calibrate ang pagsisiyasat at metro ayon sa mga tagubilin sa pabrika. Maaaring kailanganin mong i-calibrate ang metro gamit ang isang sangkap na may kilalang halaga ng PH. Ang metro ay maaaring iakma ayon sa sangkap na iyon. Kung susubukan mo ang tubig sa labas ng isang lab, inirerekumenda na isagawa mo ang pagkakalibrate na ito ng ilang oras bago ang pagsubok sa bukid. - Hugasan ang probe ng malinis na tubig bago gamitin. Patuyuin ng malinis na tela.
 Kumuha ng isang sample ng tubig at ibuhos ito sa isang malinis na lalagyan.
Kumuha ng isang sample ng tubig at ibuhos ito sa isang malinis na lalagyan.- Ang tubig ay dapat na may malalim na sapat upang lumubog ang dulo ng elektrod.
- Iwanan ang sample nang ilang sandali upang payagan ang temperatura na tumatag.
- Sukatin ang temperatura ng sample sa isang thermometer.
 Ayusin ang metro sa temperatura ng sample. Ang pagiging sensitibo ng pagsisiyasat ay apektado ng temperatura ng tubig, kaya't ang pagsukat ay maaari lamang maging tumpak kung ipinasok mo ang data ng temperatura.
Ayusin ang metro sa temperatura ng sample. Ang pagiging sensitibo ng pagsisiyasat ay apektado ng temperatura ng tubig, kaya't ang pagsukat ay maaari lamang maging tumpak kung ipinasok mo ang data ng temperatura.  Ilagay ang probe sa sample. Maghintay para sa metro na maabot ang balanse. Ang metro ay nasa isang matatag na estado kapag ang pagbabasa ay matatag.
Ilagay ang probe sa sample. Maghintay para sa metro na maabot ang balanse. Ang metro ay nasa isang matatag na estado kapag ang pagbabasa ay matatag.  Basahin ang pagsukat ng pH ng sample. Ang pH meter ay nagbibigay ng resulta sa isang sukat na 0-14. Kung ang tubig ay dalisay, ang halaga ay nasa paligid ng 7. Isulat ang iyong mga natuklasan.
Basahin ang pagsukat ng pH ng sample. Ang pH meter ay nagbibigay ng resulta sa isang sukat na 0-14. Kung ang tubig ay dalisay, ang halaga ay nasa paligid ng 7. Isulat ang iyong mga natuklasan.
Paraan 2 ng 3: Sa litmus paper
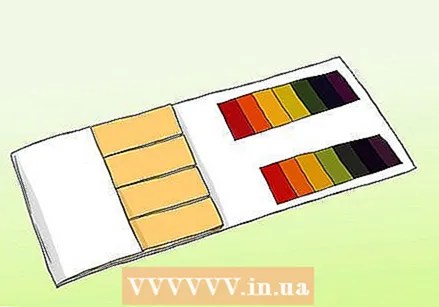 Alamin ang pagkakaiba sa pagitan ng PH paper at litmus paper. Maaari mong gamitin ang papel na PH upang makakuha ng tumpak na pagbabasa ng isang sample. Gayunpaman, ang papel na PH ay hindi dapat malito sa regular na papel na litmus. Ang pareho ay maaaring magamit upang subukan ang mga acid at base, ngunit magkakaiba ang mga ito sa mahahalagang respeto.
Alamin ang pagkakaiba sa pagitan ng PH paper at litmus paper. Maaari mong gamitin ang papel na PH upang makakuha ng tumpak na pagbabasa ng isang sample. Gayunpaman, ang papel na PH ay hindi dapat malito sa regular na papel na litmus. Ang pareho ay maaaring magamit upang subukan ang mga acid at base, ngunit magkakaiba ang mga ito sa mahahalagang respeto. - Naglalaman ang mga ph strip ng isang serye ng mga tagapagpahiwatig na nagbabago ng kulay kapag nahantad sa isang solusyon. Ang lakas ng mga acid at base sa bawat bar ay magkakaiba. Matapos ang pagbabago, ang pattern ng kulay ay maaaring ihambing sa mga halimbawang ibinigay sa kit.
- Ang papel na Litmus ay isang strip ng papel na naglalaman ng isang acid o base (alkalina). Ang pinakakaraniwang mga guhitan ay pula (na may isang acid na tumutugon sa mga base) at asul (na may isang base na tumutugon sa mga acid). Ang mga pulang guhitan ay nagiging asul kung ang sangkap ay alkalina, at ang mga asul na guhitan ay nagiging pula kung ang sangkap ay acidic. Ang mga papel na Litmus ay maaaring magamit bilang isang mabilis at madaling pagsubok, ngunit ang pinakamurang mga pagkakaiba-iba ay hindi laging nagbibigay ng tumpak na sukat ng lakas ng solusyon.
 Kumuha ng isang sample ng tubig at ibuhos ito sa isang malinis na lalagyan. Ang tubig ay dapat na may malalim na sapat upang lumubog ang strip.
Kumuha ng isang sample ng tubig at ibuhos ito sa isang malinis na lalagyan. Ang tubig ay dapat na may malalim na sapat upang lumubog ang strip.  Isawsaw ang isang test strip sa sample. Ang pagkakalantad ng ilang segundo ay sapat na. Ang mga tagapagpahiwatig na bar sa papel ay magbabago ng kulay pagkatapos ng ilang sandali.
Isawsaw ang isang test strip sa sample. Ang pagkakalantad ng ilang segundo ay sapat na. Ang mga tagapagpahiwatig na bar sa papel ay magbabago ng kulay pagkatapos ng ilang sandali.  Ihambing ang dulo ng test strip sa tsart ng kulay na kasama ng papel. Ang kulay o mga kulay sa card ay dapat na tumutugma sa kulay o mga kulay sa test strip. Ang kulay ng mapa pagkatapos ay naiugnay ang mga pattern ng kulay sa mga antas ng pH.
Ihambing ang dulo ng test strip sa tsart ng kulay na kasama ng papel. Ang kulay o mga kulay sa card ay dapat na tumutugma sa kulay o mga kulay sa test strip. Ang kulay ng mapa pagkatapos ay naiugnay ang mga pattern ng kulay sa mga antas ng pH.
Paraan 3 ng 3: Pag-unawa sa PH
 Alamin kung paano tinukoy ang mga acid at base. Ang acidity at alkalinity (ang term na ginamit upang ilarawan ang mga base) ay parehong tinukoy ng mga ion ng hydrogen na ibinibigay o kinuha nila. Ang isang acid ay isang sangkap na nagbibigay ng (o "nag-abuloy") ng mga ion ng hydrogen, at ang base ay isang sangkap na sumisipsip ng labis na mga hydrogen ions.
Alamin kung paano tinukoy ang mga acid at base. Ang acidity at alkalinity (ang term na ginamit upang ilarawan ang mga base) ay parehong tinukoy ng mga ion ng hydrogen na ibinibigay o kinuha nila. Ang isang acid ay isang sangkap na nagbibigay ng (o "nag-abuloy") ng mga ion ng hydrogen, at ang base ay isang sangkap na sumisipsip ng labis na mga hydrogen ions.  Maunawaan ang scale ng pH. Ginamit ang numero ng pH upang masukat ang antas ng kaasiman o alkalinity ng mga sangkap na natutunaw sa tubig. Karaniwan ang tubig ay may parehong dami ng mga hydroxide ions (OH−) at hydronium ions (H3O +). Nagbabago ang ratio ng mga hydroxide at hydronium ions kapag idinagdag sa tubig ang isang acidic o alkaline na sangkap.
Maunawaan ang scale ng pH. Ginamit ang numero ng pH upang masukat ang antas ng kaasiman o alkalinity ng mga sangkap na natutunaw sa tubig. Karaniwan ang tubig ay may parehong dami ng mga hydroxide ions (OH−) at hydronium ions (H3O +). Nagbabago ang ratio ng mga hydroxide at hydronium ions kapag idinagdag sa tubig ang isang acidic o alkaline na sangkap. - Karaniwan itong itinuturing na isang sukat na tumatakbo mula 0 hanggang 14 (bagaman ang mga sangkap ay maaaring mahulog sa labas ng saklaw na ito). Ang mga neutral na sangkap ay nagmamarka ng tungkol sa 7, ang mga acidic na sangkap ay nasa ilalim ng 7 at mga alkalina na sangkap sa itaas ng 7.
- Ang sukat ng PH ay logarithmic, nangangahulugang ang mga pagkakaiba sa integer ay kumakatawan sa isang sampung-tiklop na pagkakaiba sa kaasiman o alkalinity. Halimbawa, ang isang sangkap na may ph na 2 ay sampung beses na mas acidic kaysa sa isang sangkap na may pH na 3, at 100 beses na mas acidic kaysa sa isang sangkap na may isang ph na 4. Ang sukat ay gumagana sa parehong paraan sa mga alkaline na sangkap, sa anumang integer pagiging kumakatawan sa isang sampung beses na pagkakaiba.
 Alamin kung bakit sinubukan namin ang ph ng tubig. Ang purong tubig ay may pH na 7, ngunit ang Dutch tap water ay karaniwang may pH na nasa pagitan ng 7.5 at 8.3. Tunay na acidic na tubig (tubig na may mababang halaga ng PH) ay mas malamang na matunaw ang mga nakakalason na kemikal. Maaari nitong madumhan ang tubig at gawin itong hindi ligtas na maiinom.
Alamin kung bakit sinubukan namin ang ph ng tubig. Ang purong tubig ay may pH na 7, ngunit ang Dutch tap water ay karaniwang may pH na nasa pagitan ng 7.5 at 8.3. Tunay na acidic na tubig (tubig na may mababang halaga ng PH) ay mas malamang na matunaw ang mga nakakalason na kemikal. Maaari nitong madumhan ang tubig at gawin itong hindi ligtas na maiinom. - Sa pangkalahatan, pinapayuhan na subukan ang ph sa site. Kung kukuha ka ng isang sample ng tubig para sa pagsasaliksik sa lab, ang carbon dioxide (CO2) mula sa hangin ay maaaring matunaw sa tubig. Ang natutunaw na carbon dioxide ay tumutugon sa mga ions sa tubig at nagdaragdag ng kaasiman sa pangunahing o walang kinikilingan na mga solusyon. Upang maiwasan ang kontaminasyon ng carbon dioxide, ang tubig ay dapat masubukan sa loob ng dalawang oras na koleksyon.