May -Akda:
Christy White
Petsa Ng Paglikha:
8 Mayo 2021
I -Update Ang Petsa:
1 Hulyo 2024

Nilalaman
- Upang humakbang
- Paraan 1 ng 3: Unang Bahagi: Pag-unawa sa Mga Shell ng Electron
- Paraan 2 ng 3: Ikalawang Bahagi: Paghahanap ng Mga Electron ng Valence sa Mga Metal, Maliban sa Mga Transition Metal
- Pamamaraan 3 ng 3: Ikatlong Bahagi: Paghahanap ng Mga Elektrong Valence sa Mga Transition Metal
- Mga Tip
- Mga kailangan
Ang mga electron ng Valence ay nakahiga sa panlabas na shell ng isang elemento. Ang bilang ng mga electron ng valence sa isang atom ay tumutukoy sa uri ng bond ng kemikal na maaaring mabuo ng elementong ito. Ang pinakamahusay na paraan upang malaman ang bilang ng mga electron ng valence ay ang paggamit ng pana-panahong talahanayan ng mga elemento.
Upang humakbang
Paraan 1 ng 3: Unang Bahagi: Pag-unawa sa Mga Shell ng Electron
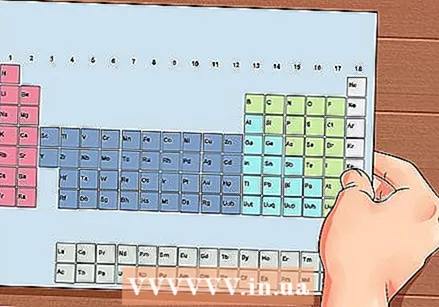 Ang Panahong Panahon ng Mga Sangkap. Ito ay isang talahanayan na may mga code ng kulay, kung saan sa bawat cell ang isang elemento ay ipinapakita na may numero ng atomic at 1 hanggang 3 titik bilang isang simbolo.
Ang Panahong Panahon ng Mga Sangkap. Ito ay isang talahanayan na may mga code ng kulay, kung saan sa bawat cell ang isang elemento ay ipinapakita na may numero ng atomic at 1 hanggang 3 titik bilang isang simbolo. 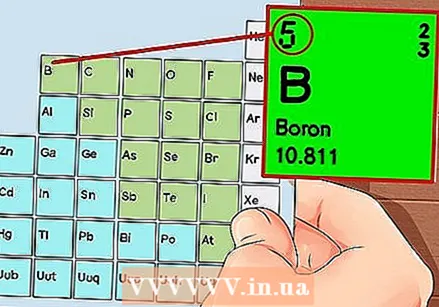 Hanapin ang bilang ng atomiko ng elemento. Ang bilang ng atomiko ay nasa itaas o sa tabi ng simbolo ng elemento. Halimbawa: Ang Boron (B) ay may isang atomic na bilang ng 5, na nangangahulugang mayroon itong 5 proton at 5 electron.
Hanapin ang bilang ng atomiko ng elemento. Ang bilang ng atomiko ay nasa itaas o sa tabi ng simbolo ng elemento. Halimbawa: Ang Boron (B) ay may isang atomic na bilang ng 5, na nangangahulugang mayroon itong 5 proton at 5 electron. 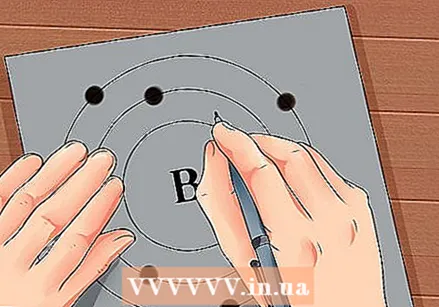 Gumuhit ng isang simpleng representasyon ng isang atom at ilagay ang mga electron sa orbit sa paligid ng nucleus. Ang mga trabahong ito ay tinatawag ding mga antas ng shell o enerhiya. Ang maximum na bilang ng mga electron na maaaring nasa parehong shell ay naayos, at ang mga shell ay napunan mula sa panloob hanggang sa panlabas na orbit.
Gumuhit ng isang simpleng representasyon ng isang atom at ilagay ang mga electron sa orbit sa paligid ng nucleus. Ang mga trabahong ito ay tinatawag ding mga antas ng shell o enerhiya. Ang maximum na bilang ng mga electron na maaaring nasa parehong shell ay naayos, at ang mga shell ay napunan mula sa panloob hanggang sa panlabas na orbit. - K Shell (panloob): 2 electron maximum.
- L Shell: 8 electron maximum.
- M Shell: 18 electron maximum.
- N Shell: 32 electron maximum.
- O Shell: 50 electron maximum.
- P Shell (panlabas): 72 electron maximum.
 Hanapin ang bilang ng mga electron sa panlabas na shell. Ito ang mga valence electron.
Hanapin ang bilang ng mga electron sa panlabas na shell. Ito ang mga valence electron. - Kapag puno ang valence shell, ang elemento ay matatag.
- Kung ang valence shell ay hindi puno kung gayon ang elemento ay reaktibo, na nangangahulugang maaari itong maiugnay ng chemically sa atom ng ibang elemento. Ang bawat atom ay nagbabahagi ng mga valence electron na ito sa pagtatangkang gawing puno ang valence shell.
Paraan 2 ng 3: Ikalawang Bahagi: Paghahanap ng Mga Electron ng Valence sa Mga Metal, Maliban sa Mga Transition Metal
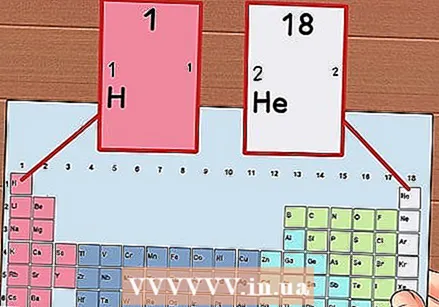 Bilangin ang bawat haligi ng periodic table, mula 1 hanggang 18. Ang Hydrogen (H) ay nasa tuktok ng haligi 1 at Helium (He) sa tuktok ng haligi 18. Ito ang magkakaibang mga grupo ng mga elemento.
Bilangin ang bawat haligi ng periodic table, mula 1 hanggang 18. Ang Hydrogen (H) ay nasa tuktok ng haligi 1 at Helium (He) sa tuktok ng haligi 18. Ito ang magkakaibang mga grupo ng mga elemento. 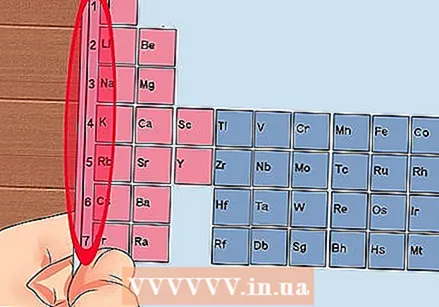 Bigyan ang bawat hilera ng isang numero, mula 1 hanggang 7. Ito ang mga panahon ng mga elemento, at tumutugma ito sa bilang ng mga shell o antas ng enerhiya ng isang atom.
Bigyan ang bawat hilera ng isang numero, mula 1 hanggang 7. Ito ang mga panahon ng mga elemento, at tumutugma ito sa bilang ng mga shell o antas ng enerhiya ng isang atom. - Ang Hydrogen (H) at Helium (He) ay parehong may 1 shell, habang ang Francium (Fr) ay mayroong 7.
- Ang mga lanthanide at actinide ay naka-grupo at nakalista sa ibaba ng pangunahing talahanayan. Ang lahat ng mga lanthanide ay nabibilang sa Panahon 6, Pangkat 3 at lahat ng mga aktinide ay kabilang sa Panahon 7, Pangkat 3.
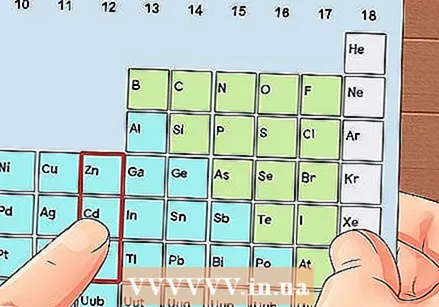 Maghanap ng isang elemento na hindi isang metal na paglipat. Ang mga metal sa paglipat ay nasa mga pangkat 3 hanggang 12. Ang mga bilang ng pangkat ng iba pang mga metal ay nagpapahiwatig ng bilang ng mga electron ng valence.
Maghanap ng isang elemento na hindi isang metal na paglipat. Ang mga metal sa paglipat ay nasa mga pangkat 3 hanggang 12. Ang mga bilang ng pangkat ng iba pang mga metal ay nagpapahiwatig ng bilang ng mga electron ng valence. - Pangkat 1: 1 valence electron
- Pangkat 2: 2 mga electron ng valence
- Pangkat 13: 3 mga electron ng valence
- Pangkat 14: 4 na mga electron ng valence
- Pangkat 15: 5 mga electron ng valence
- Pangkat 16: 6 na mga electron ng valence
- Pangkat 17: 7 mga electron ng valence
- Pangkat 18: 8 mga electron ng valence - maliban sa Helium, na mayroong 2
Pamamaraan 3 ng 3: Ikatlong Bahagi: Paghahanap ng Mga Elektrong Valence sa Mga Transition Metal
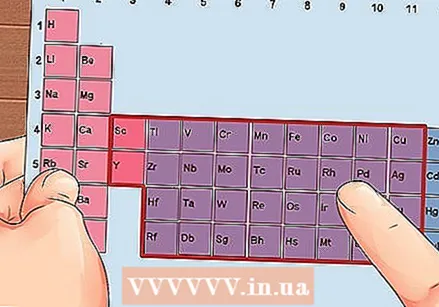 Maghanap ng isang elemento mula sa mga pangkat 3 hanggang 12, ang mga metal na paglipat.
Maghanap ng isang elemento mula sa mga pangkat 3 hanggang 12, ang mga metal na paglipat. Tukuyin ang bilang ng mga electron ng valence batay sa bilang ng pangkat. Ang mga numero ng pangkat na ito ay tumutugma sa isang posibleng bilang ng mga electron ng valence.
Tukuyin ang bilang ng mga electron ng valence batay sa bilang ng pangkat. Ang mga numero ng pangkat na ito ay tumutugma sa isang posibleng bilang ng mga electron ng valence. - Pangkat 3: 3 mga electron ng valence
- Pangkat 4: 2 hanggang 4 na mga electron ng valence
- Pangkat 5: 2 hanggang 5 mga electron ng valence
- Pangkat 6: 2 hanggang 6 na mga electron ng valence
- Pangkat 7: 2 hanggang 7 mga electron ng valence
- Pangkat 8: 2 o 3 mga electron ng valence
- Pangkat 9: 2 o 3 mga electron ng valence
- Pangkat 10: 2 o 3 mga electron ng valence
- Pangkat 11: 1 o 2 mga electron ng valence
- Pangkat 12: 2 mga electron ng valence
Mga Tip
- Ang mga metal sa paglipat ay maaaring magkaroon ng mga shell ng valence na hindi kumpleto. Ang pagtukoy ng eksaktong bilang ng mga electron ng valence sa mga metal na paglipat ay nangangailangan ng ilang mga prinsipyo ng teoryang kabuuan na lampas sa saklaw ng papel na ito.
Mga kailangan
- Panahon ng talahanayan ng mga elemento
- Lapis
- Papel